Indice
Questo recente studio prende in esame la perdita delle informazioni epigenetiche, e come questa sembri influire sull’accelerazione dei processi di invecchiamento.
La perdita di informazioni epigenetiche e l'invecchiamento
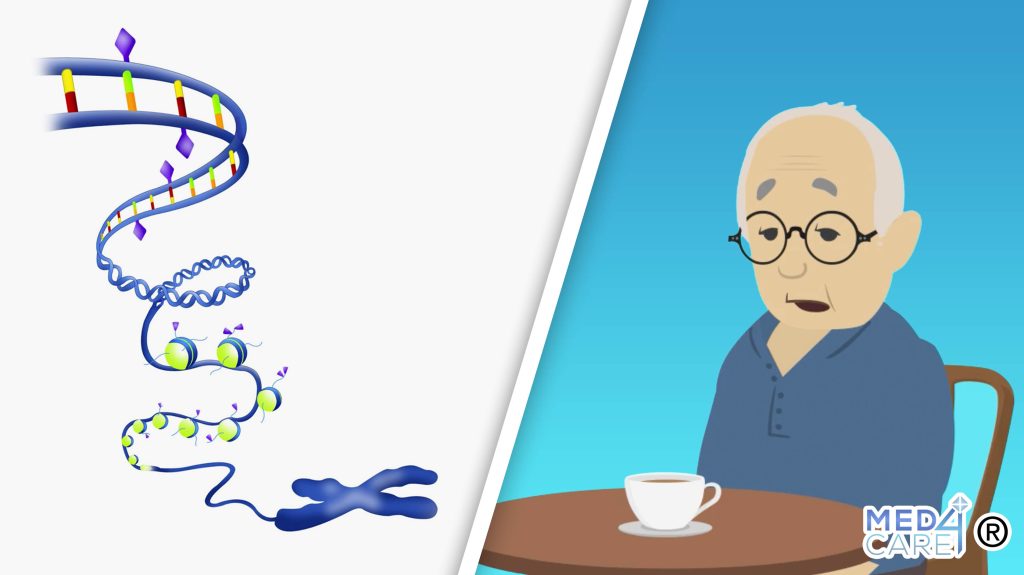
Tutti i meccanismi cellulari e il funzionamento globale dell’organismo sono diretti dall’insieme delle informazioni genetiche custodite nel DNA nucleare¹ delle cellule, che nel complesso formano il genoma.
Mentre il genoma è un termine conosciuto ai più, l’epigenoma è invece un concetto abbastanza “oscuro” e forse non approfondito a dovere.
Epigenoma e genoma
Volendo fare una metafora, se il genoma costituisce il libretto delle istruzioni che l’organismo ha a disposizione per il funzionamento delle sue cellule, l’epigenoma indica quando e in quale modalità questo libretto deve essere letto e interpretato.
L’epigenomica è infatti quella disciplina che studia le modificazioni non permanenti a livello del DNA nucleare, analizzando come questo interferisca con l’espressione dei singoli geni.
Mentre il genoma custodito all’interno di ogni cellula nucleata è lo stesso, ciò che varia è l’epigenoma ossia il modo con cui i geni possono essere espressi o silenziati, in funzione delle richieste contingenti della cellula e degli stimoli esterni.
Diversi studi si stanno concentrando sul fatto che il processo di invecchiamento è quasi sempre contraddistinto da una perdita lenta e inesorabile di informazioni epigenetiche e questo fenomeno impatta notevolmente sulla longevità. [1]
Caratteristiche dello studio
- Tipo di studio: Studio sperimentale condotto in laboratorio.
- Luogo: Stati Uniti, Giappone.
Scopo dello studio: la perdita di informazioni epigenetiche accelera l'invecchiamento?
Gli autori dello studio hanno tentato di comprendere come le variazioni a livello epigenetico possano interferire con i processi di invecchiamento nei mammiferi.
Progettazione dello studio
Lo studio è globalmente molto complesso e si basa sull’induzione di modifiche all’epigenoma in topi transgenici, denominati topi ICE (Inducible Changes to the Epigenome).
In questi topi si è provveduto alla fusione di un gene proveniente da un protista, denominato I-Ppol, con due geni murini regolati dal tamoxifene, di cui uno ricombinato, definiti come ERT2 e Cre-ERT2.
I topi transgenici con Cre-ERT2 e con ERT2-I-Ppol sono stati designati come topi ICE mentre i topi con geni wild hanno funzionato da controllo.
Tutti i topi coinvolti nell’esperimento sono stati quindi sottoposti a vari test, come:
- Il test di condizionamento alla paura;
- La prova del tapis roulant;
- Il test del labirinto di Barnes;
- Misurazione dei livelli di lattato.
Al termine di questi test, dopo l’esecuzione di ulteriori micro-procedure e il post-trattamento, i ricercatori hanno analizzato la cromatina e alcuni regolatori epigenomici in vari distretti cellulari dei topi testati.
Risultati
I risultati dello studio sono stati effettuati comparando i topi ICE, ovvero i topi in cui sono state indotte variazioni sull’epigenoma, con i topi wild.
Sono emerse le seguenti interessanti considerazioni:
- Le cellule studiate nei topi ICE sono risultate circa 1 volta e mezzo “più vecchie” rispetto al controllo.
- Le cellule studiate nei topi ICE sono risultate essere più sensibili ai danni al DNA.
- Dopo 10 mesi i topi ICE hanno mostrato segni palesi di invecchiamento nella pelle, nei muscoli, nel cervello e nei reni.
Conclusioni: l'invecchiamento sembra essere accelerato dalla perdita di informazioni epigenetiche
Lo studio di cui riferiamo ha messo in luce che la perdita delle informazioni epigenetiche, magari indotta da un danno alla doppia elica del DNA, accelera i processi di invecchiamento e le malattie legate all’età nei topi.
Tuttavia pare che i mammiferi possano accedere a una sorta di “copia di back-up” delle informazioni epigenetiche giovanili e tramite queste ripristinare la funzionalità dei tessuti invecchiati.
Sono necessari ulteriori e più approfonditi studi per comprendere al meglio questo interessante fenomeno di (dis)regolazione epi-genomica.
Bibliografia: fonti e note
ARTICOLO ORIGINALE: Yang J-H, Hayano M, Griffin PT et al. Loss of epigenetic information as a cause of mammalian aging. Cell. 2023;186(2).
[1] Kane AE, Sinclair DA. Epigenetic changes during aging and their reprogramming potential. Crit Rev Biochem Mol Biol. 2019 Feb;54(1):61-83.
Nota 1. Nella sua accezione più larga il genoma comprende anche le informazioni genetiche del DNA mitocondriale, del DNA plasmidico nei batteri, così come di quello dei cloroplasti nelle piante e nelle alghe.