Miastenia gravis: cause, sintomi e trattamento
Esiste una famiglia di malattie neurologiche che prende il nome di “Sindromi miasteniformi”, la quale riguarda un particolare distretto neurologico: la giunzione neuromuscolare. In questa piccola sede avviene il passaggio dell’impulso elettrico dal nervo al muscolo per la contrazione.
Successivamente entreremo nel dettaglio di quali siano le componenti di questa struttura e allo stesso tempo quali possano essere i foci o le alterazioni che riguardano le diverse strutture nell’ambito della giunzione neuromuscolare che possono portare alla sindrome miasteniforme.
Cos’è la Miastenia Gravis?
La miastenia gravis è una malattia autoimmune abbastanza rara in cui sono presenti degli anticorpi che si legano ai recettori per l’acetilcolina nella membrana postsinaptica della giunzione neuromuscolare. (1) Gli anticorpi in questione determinano un blocco dei recettori per l’acetilcolina, che non funzionano più a dovere. La acetilcolina è un neurotrasmettitore muscolare e quando cerca di raggiungere il proprio recettore, trovandolo bloccato dall’anticorpo, non è in grado di svolgere la propria funzione di mediare una valida attività muscolare. Questo si traduce, a livello clinico, cioè di sintomi visibili, in un’affaticabilità muscolare in diversi distretti corporei.
Attenzione! Autoimmune vs Immunomediata!
La miastenia gravis rappresenta un esempio di vera malattia autoimmune. A volte per definire le malattie prodotte dal coinvolgimento del sistema immunitario si parla erroneamente di malattia autoimmune quando in realtà abbiamo a che fare con malattie immunomediate. La stessa sclerosi multipla, per esempio, è una malattia immunomediata, così come l’artrite reumatoide, mentre la miastenia è una vera malattia autoimmune, in quanto è presente l’identificazione dell’anticorpo e quindi anche dell’antigene coinvolto in questo disturbo autoimmune.
La miastenia gravis costituisce il più comune disturbo della giunzione neuromuscolare ed è una delle malattie neurologiche che può essere però trattata con successo, per quanto essa sia comunque cronica e ad andamento lentamente ingravescente e non scevro da complicanze anche fatali.
Epidemiologia della Miastenia gravis
- E’ una malattia piuttosto rara
- La forma più comune è quella legata agli anticorpi contro il recettore per l’acetilcolina
- L’incidenza della miastenia gravis varia da 1 soggetto su 1 milione di abitanti a 15/milione, con una media di 5,3 soggetti per milione di abitanti
- Per quanto riguarda la popolazione maschile, si nota un aumento dell’incidenza dai 50-60 anni in su (un picco)
- L’incidenza nella popolazione femminile, invece, è più alta tra i 20-29 anni e poi in età avanzata, con una distribuzione a 2 picchi.
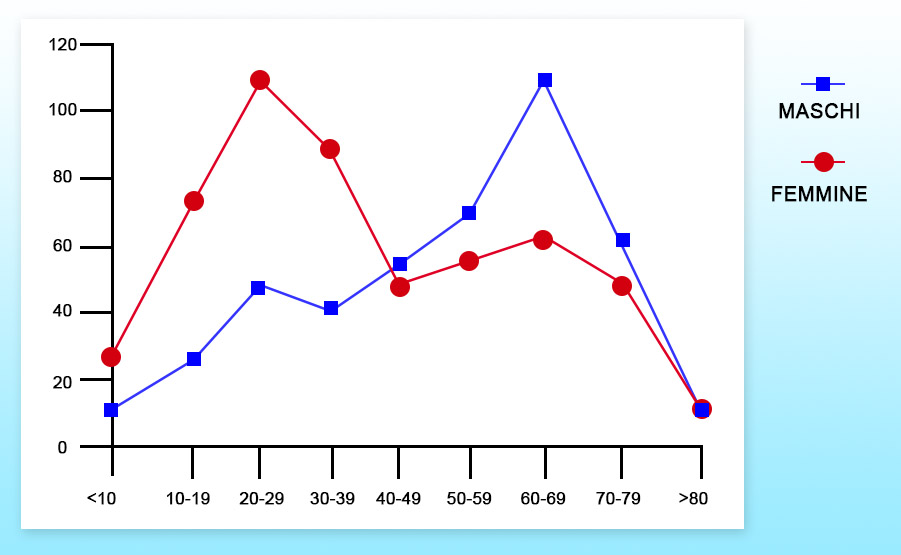
- E’ una malattia cronica, quindi è una malattia di cui raramente si muore – può accorciare l’aspettativa di vita, ma non rappresenta la causa di morte dei soggetti portatori della malattia.
Fisiopatologia della miastenia gravis
Con il termine “miastenia gravis” ci riferiamo alla malattia autoimmune che produce autoanticorpi contro la placca neuromuscolare, nella maggior parte dei casi contro il recettore per l’acetilcolina che è esposto sul versante delle cellule muscolari della placca. Per capire meglio il fenomeno rivediamo come è strutturata la giunzione, o placca, neuromuscolare.
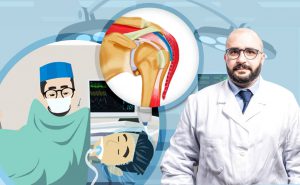
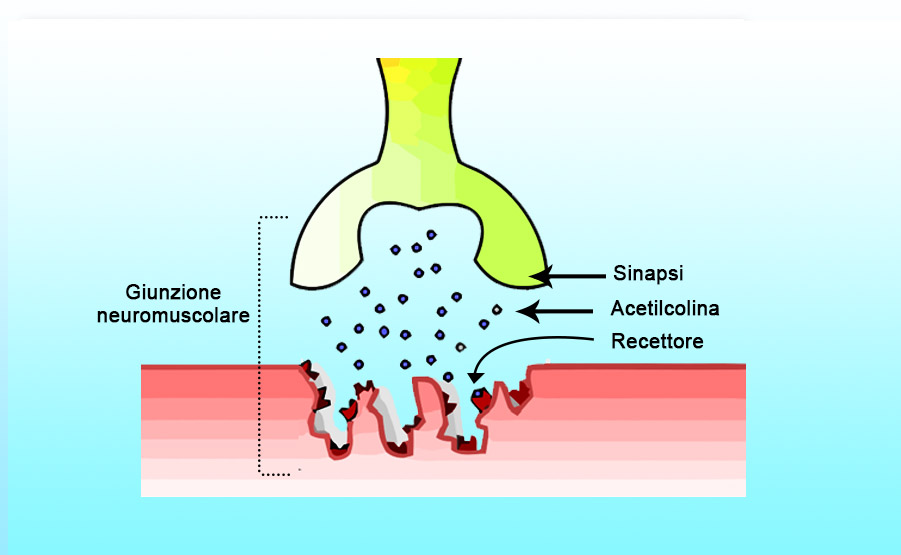
La struttura della giunzione neuromuscolare
La giunzione sinaptica neuromuscolare, detta anche placca neuromuscolare, è costituita da due elementi. Il primo è il neurone motorio, o motoneurone, con tutte le vescicole sinaptiche che contengono l’acetilcolina. Il motoneurone prende rapporto con la seconda struttura, la cellula muscolare, che ha una superficie caratterizzata da invaginazioni. Le due componenti, neuronale e muscolare, si affacciano una all’altra come le sponde di un fiume, lasciando tra loro uno spazio nel quale si muovono i neurotrasmettitori come l’acetilcolina.
Sulla superficie muscolare ci sono dei recettori, che aggettano sullo spazio sinaptico, pronti a ricevere l’acetilcolina. Quest’ultima viene liberata dalle vescicole al momento dell’arrivo del potenziale d’azione nel neurone. L’acetilcolina è liberata nello spazio postsinaptico, lo attraversa come una barca attraversa il fiume e si reca dell’altra parte della riva, dove trova la cellula muscolare che presenta il recettore per l’acetilcolina. Il legame tra il neurotrasmettitore e il recettore scatena il meccanismo di eccitazione-contrazione della fibra muscolare, di conseguenza è essenziale per la contrazione della fibrocellula muscolare.
I bersagli della miastenia gravis sulla placca neuromuscolare
Il recettore per l’acetilcolina presente sul versante muscolare della placca neuromuscolare è il principale bersaglio della malattia. Auto-anticorpi vengono prodotti contro di esso, che in tal modo risulta non funzionante in modo corretto.
Questo è il meccanismo che nell’80% dei casi risulta alterato, quindi è il meccanismo che rappresenta la base dell’alterazione nella miastenia gravis per l’80% dei casi.
Tuttavia, vi sono altre strutture che possono essere antigeni e quindi target di una risposta autoanticorpale che interagisce con la funzione neuromuscolare:
- Enzimi come la chinasi specifica del muscolo e il recettore correlato al peptide 4 della lipoproteina che si trova sulla membrana postsinaptica
- Dei recettori per la rianodina, i quali si trovano invece sulla membrana sarcoplasmatica, che contribuiscono anche questi alla contrazione del muscolo. Sebbene in forme molto più rare anche verso questi recettori possono formarsi degli anticorpi.
- Autoanticorpi diretti contro la titina
Queste sopra elencate sono le principali sedi di alterazione della placca neuromuscolare a livello delle quali si genera una forma di affaticabilità muscolare, autoimmune perchè generata da auto-anticorpi, detta anche miastenia gravis o sindrome miasteniforme.
Il meccanismo d’azione degli auto-anticorpi contro la placca neuromuscolare
In che modo gli auto-anticorpi diretti contro il recettore dell’acetilcolina sono in grado di determinare l’alterazione alla base della malattia? Si possono identificare due meccanismi principali:
- Blocco della funzione per ingombro (sterico): l’anticorpo esercita una forma di blocco fisico nei confronti dell’acetilcolina, perchè legandosi esso per primo impedisce il legame acetilcolina-recettore;
- Formazione di un’infiammazione cronica: il legame antigene-anticorpo, come sempre accade, determina un’infiammazione cronica, mediata dal sistema immunitario, a carico della superficie cellulare attorno al recettore in questione. Con l’andar del tempo le cellule tendono a reagire all’infiammazione cronica, cercando di eliminare il suo fattore scatenante, perciò riducono la formazione di pliche o inducono una semplificazione delle stesse, in modo tale che si abbia una riduzione della densità dei recettori e quindi di infiammazione. Questo meccanismo è utilizzato dalla cellula per proteggere la propria integrità ed evitare l’infiammazione cronica, tuttavia tende a peggiorare i sintomi della malattia, perchè riduce ulteriormente la quantità di recettori e quindi il funzionamento corretto dell’acetilcolina e della placca neuromuscolare.
Meccanismo di produzione degli auto-anticorpi nella miastenia gravis
Chi produce gli anticorpi per il recettore dell’acetilcolina? Il principale indiziato, per lo meno nella maggior parte dei casi, è una ghiandola che fa parte del sistema immunitario, il timo, spesso alterato in questa patologia.
Il timo di norma va incontro ad involuzione completa nel soggetto adulto, ma può presentare alcune forme alterate:
- Nella forma da iperplasia timica, tipica delle donne giovani, continua invece a presentare delle funzioni. Nell’iperplasia il tessuto è ricco di follicoli linfoidi multipli con centri germinativi che producono anticorpi (2) contro un antigene interno al nostro organismo, in questo caso il recettore dell’acetilcolina. In questi casi specifici, tipici appunto della donna giovane, sembrerebbe che il timo non vada mai incontro ad una involuzione completa, ma persista sotto forma di iperplasia, quindi un’architettura errata della ghiandola con la presenza di follicoli linfoidi multipli, a sua volta responsabili della produzione di auto-anticorpi.
- Altra situazione invece quella che colpisce sia la donna anziana sia l’uomo anziano che riguarda il timoma, un tumore benigno, quindi che si manifesta in un timo che è andato regolarmente incontro ad involuzione come avverrebbe nell’adulto normale, ma che ad un certo punto presenta dei cloni di cellule che si riproducono in modo più o meno differenziato. (3)
Gli anticorpi anti-AchR, presenti nella maggioranza dei casi di miastenia
Il meccanismo alla base della produzione di autoanticorpi si basa sull’attività delle cellule immunitarie T CD4+: esse presentano gli antigeni self durante lo sviluppo e porterebbero all’attivazione di plasmacellule periferiche produttrici degli autoanticorpi verso antigeni self.
Gli anticorpi anti-recettore per l’acetilcolina hanno la sigla Ab anti-AchR e si possono dosare nel sangue per consentire una diagnosi specifica della malattia (5).
Assenti nei soggetti sani, sono invece presenti nell’80% della miastenia gravis generalizzata e nel 70% della forma oculare.
Sintomatologia della Miastenia gravis
Affaticabilità
Il meccanismo della riduzione della trasmissione neuromuscolare dà luogo a una esauribilità della contrazione muscolare, che si traduce sul piano clinico in una forma di affaticabilità: il paziente sviluppa fatica muscolare con l’esercizio fisico, inteso non come sport, ma come azioni di base che vengono messe in gioco da un distretto muscolare.
Nota: differente è il concetto di fatica muscolare, un sintomo che il paziente lamenta già dalle prime ore del mattino e che in genere si associa alle miopatie primitive, quindi alla presenza di disordini del muscolo di tipo primitivo o secondario.
Il distretto più frequente soprattutto all’esordio è quello della muscolatura oculare estrinseca. E’ presente nel 60% dei casi all’esordio di malattia ed nel 90% dei casi durante il corso generale della malattia. L’affaticabilità a carico della muscolatura estrinseca dell’occhio si traduce in altri due sintomi, la diplopia e la ptosi palpebrale.
Diplopia
La diplopia nella miastenia gravis è dovuta alla faticabilità della muscolatura estrinseca dell’occhio: movimenti oculari dei muscoli estrinseci dell’occhio, ovvero quelli innervati dal terzo paio di nervi cranici, dal quarto e dal sesto, perciò l’oculomotore comune, il trocleare e l’abducente. Questi muscoli agiscono in sinergia, per tenere ad esempio lo sguardo in posizione primaria su un oggetto e fare in modo che lo stesso oggetto cada su punti corrispondenti della retina e l’immagine venga perciò fusa a livello corticale.
Nel caso della diplopia dopo un affaticamento, che può essere per esempio una lettura prolungata oppure una fissazione prolungata, un viaggio in macchina oppure guardare la televisione, si ha un’affaticabilità asimmetrica a carico dei muscoli estrinseci dell’occhio, quindi un disassamento a carico dei bulbi oculari con la proiezione dell’oggetto su punti non corrispondenti della retina che il cervello non riesce a fondere e che percepisce quindi come doppi.
Ptosi palpebrale
La ptosi palpebrale nella miastenia è determinata dal fatto che anche il muscolo elevatore della palpebra fa parte dell’innervazione del terzo paio di nervi cranici, ovvero l’oculomotore comune. Con l’affaticamento che si può indurre anche durante l’esame obiettivo questi pazienti presentano una caduta della palpebra sull’occhio.
Riassumendo, è importante ricordare che diplopia e ptosi palpebrale sono spesso i sintomi d’esordio della miastenia gravis.
Il 15% delle miastenie sono solo forme oculari, perciò vengono definite miastenie oculari.
Le miastenie oculari generalmente hanno un andamento più benigno, rispondono alla terapia, ma possono essere comunque fastidiose.
Disfagia e sintomatologia della miastenia dovuta alla muscolatura bulbare
Nella miastenia gravis può essere presente la disfagia, espressione del coinvolgimento della muscolatura bulbare, cioè da una affaticabilità a carico delle funzioni muscolari bulbari. Gli altri effetti dell’interessamento della muscolatura bulbare emergono nelle altre funzioni di:
- Deglutizione
- Masticazione
- fonazione, anche con modifica del timbro della voce, che tende a diventare nasale.
La disfagia è in genere a carico di cibi liquidi, mentre la difficoltà nella masticazione riguarda soprattutto cibi che richiedono una masticazione prolungata come la carne.
Altri sintomi neurologici di miastenia bulbare
Tra gli altri sintomi della miastenia bulbare abbiamo:
- Ipofonia
- Una forma di disartria, che compare durante la fonazione, quindi durante l’eloquio soprattutto se protratto.
Il problema della muscolatura bulbare è che in quest’ambito dobbiamo anche annoverare la muscolatura respiratoria, di conseguenza abbiamo un’affaticabilità della muscolatura respiratoria, la quale coinvolge sia i muscoli intercostali sia soprattutto il diaframma, e può portare ad un’insufficienza respiratoria. In questo caso si parla di crisi miastenica. L’insufficienza respiratoria può caratterizzare le forme più complesse e croniche di miastenia gravis.
La crisi miastenica come sintomo di emergenza nella miastenia gravis
La crisi miastenica è l’emergenza che il neurologo o il rianimatore devono riconoscere ed affrontare per salvare la vita al paziente. Si tratta del coinvolgimento nell’affaticamento dei muscoli del torace superiore. E’ possibile la paralisi respiratoria con una grave insufficienza respiratoria che può necessitare di trattamento intensivo, ventilazione invasiva con intubazione tracheale.
Le forme generalizzate di miastenia gravis comprendono sia l’interessamento della forma muscolare oculare estrinseca sia della muscolatura bulbare sia di quella assiale degli arti.
Siccome nella sindrome è coinvolto il recettore per l’acetilcolina, che è un neurotrasmettitore della muscolatura scheletrica, sono risparmiate in questo caso la muscolatura liscia e la muscolatura cardiaca, per cui non vi sono sintomi a carico del sistema vegetativo, gastrointestinale e cardiaco.
Esordio della patologia
L’esordio è subdolo oppure può essere precipitato da un evento scatenante, come può essere:
- Comparsa di una febbre. L’aumento della temperatura in genere peggiora i sintomi
- Turbamento emotivo
- Gravidanza
- Puerperio
Sottogruppi della Miastenia Gravis (6)
- Forme early onset (ad esordio precoce): caratterizzate dalla presenza di anticorpi per i recettori dell’Ach, hanno un’età d’insorgenza sotto i 50 anni e sono spesso associate ad iperplasia del timo
- Forme late onset (ad esordio tardivo) insorgono dopo i 50 anni e comunemente sviluppano un’atrofia del timo
- Timoma: forma considerata paraneoplastica, si può sviluppare a qualsiasi età. Nel timoma troviamo anticorpi per i recettori dell’Ach ed è associato a linfoepiteliomi.
Esistono poi forme da anticorpi contro la chinasi specifica del muscolo, che si sviluppano a qualsiasi età e presentano un timo normale.
- Forme sieronegative: così chiamate perché non vi sono anticorpi dosabili nel siero. L’interessamento del timo è variabile, con forme di timoma più o meno differenziato
- Forma oculare: ha anticorpi variabili, spesso anti-recettore, può colpire a tutte le età e il timo ha caratteristiche variabili
A queste diverse forme sono associate diverse predisposizioni, sulla base di aplotipi HLA (7):
- Forma ad esordio precoce, che coinvolge soprattutto soggetti che presentano positività per l’HLA DR3, B8 e geni non HLA
- Forma ad esordio tardivo, la quale ha HLA DR2, B7 e DBR1 15.01, che possono essere ritrovati in altre patologie autoimmuni e in specifiche popolazioni, come quella sarda
- Anticorpi anti-titina e anti-recettore per la rianodina si associano a forme severe di malattia, con anche possibile riduzione della risposta alla terapia. Gli anticorpi anti-MuSK li ritroviamo soprattutto in popolazioni del Mediterraneo e sono associati a forme severe di malattia, forme bulbari e generalizzate, con sviluppo di atrofia.
Classificazione Clinica delle forme di miastenia gravis (8)
- Classe 1: esclusivamente ipostenia muscolare oculare, compresa la chiusura degli occhi
- Classe 2: ipostenia di muscoli diversi da quelli oculari, ma può coesistere con l’ipostenia oculare. Si divide in 2a e 2b. La 2a interessa principalmente la muscolatura degli arti e/o assiale, con minore coinvolgimento orofaringeo. La 2b coinvolge la muscolatura orofaringea e respiratoria e in minor misura può arrivare a quella degli arti e/o assiale.
- Classe 3: ipostenia moderata che interessa un settore diverso da quello oculare, ma può coesistere con un’ipostenia oculare di qualunque entità. Divisa in 3a e 3b con lo stesso principia della divisione della classe 2.
- Classe 4: è la forma più generalizzata, che può dare invalidità importanti. Può coinvolgere vari distretti. Ipostenia grave che interessa un distretto diverso da quello oculare, ma può coesistere con un’ipostenia oculare di qualsiasi entità. Divisa in 4a e 4b con la solita divisione.
- Classe 5: necessita di intubazione tracheale, con o senza ventilazione meccanica, ed è accompagnata da difficoltà nella deglutizione. Quindi è caratterizzata da disfagia e dispnea.
Diagnosi di Miastenia gravis
I criteri diagnostici sono:
- Clinico o anamnestico, in quanto il fulcro diagnostico è l’affaticabilità
- L’esame obiettivo neurologico è importante, perché, ad esempio nelle forme oculari, possiamo non notare alterazioni della motilità oculare a riposo, ma questo cambia dopo aver fatto affaticare il soggetto.
- Farmacologico, con la valutazione della risposta alla piridostigmina.
- Elettrofisiologico, un’elettromiografia su una singola fibra, per poter analizzare come questa si affatichi durante la contrazione
- Immunologico: ricerca nel siero di anticorpi anti-recettore. La più comune è la ricerca degli anticorpi per il recettore dell’Ach, mentre quelle per gli altri determinanti della placca neuromuscolare sono riservate a centri specifici;
- Imaging del mediastino, che può rilevare un’iperplasia timica, in cui tutto il timo assorbe il contrasto, oppure un timoma, in cui il mezzo di contrasto ha assorbimento focale.
Un tempo veniva svolto un test di affaticabilità neuromuscolare, detto di Desmedt, che era fastidioso per il paziente, perché si trattava di una ripetuta stimolazione muscolare in presenza di un’ipossia da compressione. Con un bracciale da pressione si induceva un’ipossia temporanea nel braccio e contemporaneamente si stimolava ripetutamente il muscolo, in modo da generare un affaticamento. Così osservavamo una progressiva riduzione dell’ampiezza della contrazione muscolare, testimoniando in questo modo la presenza di un’affaticabilità neuromuscolare.
Trattamento della miastenia gravis
E’ di tipo sintomatico, in quanto non risolve il meccanismo patogenetico, ma riesce a fare in modo che l’acetilcolina possa legarsi ai recettori.
Alcuni farmaci utilizzati sono:
- Inibitori dell’acetilcolinesterasi
- Cortisonici, come il prednisone e il prednisolone, che hanno effetto immunosoppressivo sulle plasmacellule e quindi sulla produzione degli stessi anticorpi.
- Immunosoppressori, come azatioprina, micofenolato mofetile, metotrexate, ciclosporina, tacrolimus e ciclofosfamide.
- Tra le più nuove opzioni terapeutiche c’è quella degli anticorpi monoclonali, come il rituximab, che ha comunque lo stesso obiettivo di ridurre la risposta immunitaria e la produzione di anticorpi
Il farmaco inibitore dell’acetilcolinesterasi usato più di frequente è la piridostigmina: viene somministrata in compresse da 60 mg.
Gli effetti collaterali del farmaco sono autonomici su base colinergica, come ad esempio bradicardia, sintomatologia vagale e diarrea. Alcuni pazienti sono particolarmente sensibili a questo farmaco e presentano numerosi di questi effetti collaterali, rendendo impossibile un aumento di dose anche se necessario. Il rischio maggiore di questo farmaco è la crisi colinergica.
Algoritmo del trattamento della miastenia gravis:
- Nel caso della miastenia gravis generalizzata, si inizia con gli inibitori dell’acetilcolinesterasi (ed eventuale timectomia solo se l’esordio precoce è associato a timoma).
- Nel caso questo primo passo porti a remissione clinica, il paziente continuerà la terapia con gli inibitori, mentre in caso contrario dovrà associare dei cortisonici o l’azatioprina.
- Se otteniamo un effetto adeguato il paziente continuerà con la dose più bassa possibile sia di inibitori che di azatioprina e prednisone.
- Se, invece, l’effetto non fosse adeguato, si passa a farmaci più importanti, come rituximab o micofenolato mofetile.
Prognosi della miastenia gravis
La prognosi è buona nell’ 80% dei pazienti, perché questi hanno delle forme poco generalizzate da anticorpi anti-recettore, oppure forme solo oculari, oppure sono donne giovani con iperplasia timica. In questi casi la terapia garantisce una prognosi buona, con qualità di vita e autonomia quasi normali. La miastenia è comunque una patologia cronica e le remissioni totali sono poche. Anche senza remissione, però, questi pazienti riescono a gestire l’affaticabilità durante la giornata. Le prognosi è peggiore per quelle forme paraneoplastiche, legate a timomi, e per le per le forme bulbari e generalizzate, associate a crisi miasteniche.

Se ti è piaciuto questo articolo e vuoi rimanere aggiornato sulle nostre prossime pubblicazioni clicca qui per iscriverti alla nostra newsletter.
Fonti e note:
- La membrana postsinaptica della giunzione neuromuscolare ovviamente è la membrana muscolare, essendo la presinaptica la membrana del bottone della terminazione nervosa.
- Sono spesso cellule della serie B.
- Chiaramente, la produzione di anticorpi da parte di queste plasmacellule avviene soprattutto nelle lesioni differenziate, nei timomi differenziati, ma può essere osservato anche nei timomi di classe maligna che possono anche metastatizzare in modo locale ed ovviamente costituire un problema un po’ diverso e più importante con prognosi diversa nel paziente.
- Classe di linfociti T che maturano per l’appunto nel Timo. “CD4” è invece una classe di proteine trans membrana dette “helper” perché “aiuta” il riconoscimento antigenico.
- In genere è un esame che richiede qualche giorno per il referto, si può fare in ambito ospedaliero ma anche da esterno.
- Studio effettuato da Nils Erik Gilhus, MD PhD, sulla popolazione norvegese di Berge.
- “Con il termine aplotipo si definisce la combinazione di varianti alleliche lungo un cromosoma o segmento cromosomico contenente loci in linkage disequilibrium, cioè strettamente associati tra di loro” (Antropologia molecolare. Manuale di base. D.Caramelli. Firenze University Press, 2009.)
- Classificazione clinica MGFA (Myasthenia Gravis Foundation of America, fondazione americana per la miastenia gravis)
- “Molecular Biology of the Cell” (Alberts B, Johnson A, Lewis J, Raff M, Roberts k, Walter P – Garland Science, 2002)
- “Skin gammadelta T-cell functions in homeostasis and wound healing” (Julie Jameson e Wendy L. Havran in Immunological Reviews, vol. 215, 2007-2)
- “An update on myasthenia gravis” (Martínez Torre S, Gómez Molinero I, Martínez Girón R.)
- “Treatment of juvenile myasthenia gravis” (Arroyo HA.)
- “Diagnosis and treatment of myasthenia gravis” (Ponseti J, Espín E, Armengol M.)
- “Basic Immunology” (Abul K. Abbas, Shiv Pillai, Andrew H. Lichtman)