Persistenza prolungata di SARS-CoV-2 RNA nei fluidi corporei
In questo articolo riportiamo un interessante studio che ha valutato 49 casi di malattia da coronavirus nel Guangdong, in Cina, al fine di stimare la frequenza e la persistenza del virus SARS-CoV-2 nei fluidi del corpo.
L’inizio dell’epidemia
Nel dicembre 2019, la malattia denominata COVID-19, causata da un nuovo coronavirus (SARS-CoV-2) capace di portare ad una grave sindrome respiratoria acuta, è emersa a Wuhan, in Cina. La sua diffusione è stata estremamente rapida, tanto che a partire dall’1 aprile 2020 il virus si è esteso a 195 paesi.
La conferma clinica e i dubbi sull’affidabilità dei tamponi
Clinicamente, la conferma dell’infezione da SARS-CoV-2 si basa sul rilevamento del virus in vari fluidi corporei, in particolare servendosi di campioni delle vie respiratorie superiori e inferiori durante la fase acuta dell’infezione.
Tuttavia, nonostante la persistenza di SARS-CoV-2 nei campioni, la frequenza con cui essa vene rilevata ed il periodo durante il quale rimane riscontrabile non sono ancora ben chiari.
È necessaria una comprensione dettagliata della dinamica delle prime fasi dell’infezione da SARS-CoV-2 per delineare al meglio i test diagnostici e gli interventi di prevenzione, poiché l’evidenza al momento disponibile si basa solo su osservazioni tratte da casi clinici.
Lo studio
Nello studio sono stati reclutati 43 pazienti con casi lievi di COVID-19 (22 maschi, 21 femmine, con età media 43 anni, intervallo 1-70 anni) e 6 pazienti con casi gravi (6 maschi; età media di 67 anni, intervallo 46-76 anni). A tutti sono stati effettuati un tampone faringeo, un tampone rinofaringeo, un prelievo di espettorato e campioni di feci ogni 3 giorni per 4 settimane.
Tutti i campioni sono stati testati con una tecnica di laboratorio (PCR real-time) per stimare il tempo necessario alla negativizzazione dei tamponi di SARS-CoV-2 . I risultati sono stati riportati in medie e 95^ percentili, espressi come numero di giorni, tra il giorno successivo l’insorgenza della malattia e il giorno del primo risultato negativo di rRT-PCR.
Dei 49 pazienti, 15 sono stati dimessi dall’ospedale dopo più di 4 settimane di osservazione.
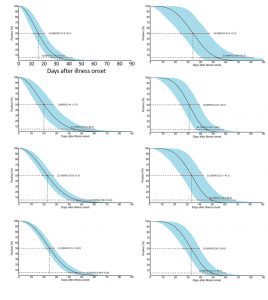
Grafico 1. Tempo fino alla clearance della sindrome respiratoria acuta grave da coronavirus in campioni di tampone faringeo, espettorato, rinofaringeo e feci tra pazienti ospedalizzati con malattia da coronavirus.
A, B) campioni di tampone faringeo da pazienti con casi lievi (A) e gravi (B);
Campioni di espettorato C, D da pazienti con casi lievi (C) e gravi (D);
Campioni di tampone rinofaringeo da pazienti con casi lievi (E) e gravi (F);
Campioni di feci G, H) da pazienti con casi lievi (G) e gravi (H).
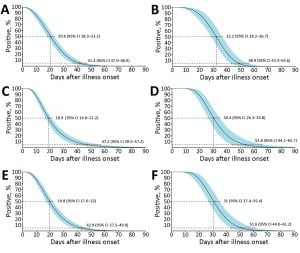
Figura 2. Tempo fino alla clearance della sindrome respiratoria acuta grave da coronavirus in campioni di tampone faringeo, espettorato, rinofaringeo e feci tra pazienti ospedalizzati con malattia da coronavirus.
A, B) regressione Weibull per casi lievi (A) e gravi (B);
C, D) regressione anomala per casi lievi (C) e gravi (D);
Regressione gamma E, F) per casi lievi (E) e gravi (F).
Sono stati testati un totale di 43 pazienti lievi e 6 con casi gravi. Sono indicate le mediane e il 95^ percentile del tempo fino alla perdita di rilevazione; barre di errore e ombreggiatura indicano IC al 95%.
I campioni
È stato prelevato un totale di 490 campioni (32,75% del numero designato di campioni, 1.006 campioni mancanti), inclusi:
- 88 campioni di tampone faringeo (23,53%, 198 campioni mancanti);
- 62 campioni di espettorato (16,58%, 312 campioni mancanti);
- 175 campioni rinofaringei (46,79%, 199 campioni mancanti);
- 165 campioni fecali (44,12%, 209 campioni mancanti).
Di questi, 171 campioni sono risultati positivi al virus, inclusi 16 campioni di tamponi faringei, 38 campioni di espettorato, 89 campioni di tampone rinofaringeo e 28 campioni di feci (Figura 1).
Considerando il tempo fino alla negativizzazione del tampone faringeo, espettorato e fecali (Tabella; Figure 1, 2), la valutazione di sensibilità e stabilità non ha mostrato differenze tra loro (Appendice Tabella, Figure 2, 3).
Conclusioni
In questo studio è stato stimato il tempo necessario ad eliminare il virus SARS-CoV-2 nella fase acuta dell’infezione.
Il tampone faringeo e di feci rilevava la presenza persistente del virus
- Casi lievi: da 45,6 giorni per campioni di tampone rinofaringeo a 46,3 giorni per campioni di feci
- Casi gravi: da 48,9 giorni per campioni di tampone rinofaringeo a 49,4 giorni per campioni di feci
In generale, dunque, un tempo più lungo di quelli di SARS-CoV e MERS-CoV.
Nonostante due studiosi abbiano rilevato casi positivi nel tampone faringeo di pazienti che si sono ripresi dall’infezione lieve da COVID-19 nei successivi 50 giorni, questo studio ha provato che dovrebbe essere un evento che difficilmente si verifica.
Inoltre, sono state trovate differenze nelle rilevazioni della presenza del virus tra i campioni dei casi lievi ma non dei casi gravi, come si può vedere nella Tabella.
Ciò non sembra sia collegato alla gravità del COVID-19, poiché in questo studio è stato utilizzato un numero limitato di campioni, eppure un test aggiuntivo ha evidenziato fenomeni simili.
Tuttavia, il tempo stimato fino alla negativizzazione dei tamponi di vari fluidi corporei in questo studio era ragionevole ed era coerente con i risultati dei casi segnalati precedentemente.
Di recente, sono state sollevate problematiche nella diagnosi molecolare di COVID-19: i campioni delle vie respiratorie superiori mostrano tassi di positività più bassi e una instabilità della presenza del virus, mentre i campioni delle vie respiratorie inferiori, come il liquido di lavaggio bronco-alveolare, sono campioni più affidabili12.
La spiegazione più probabile dei risultati discrepanti con le stime dello studio risiede nell’operazione irregolare del campionamento delle vie respiratorie superiori nelle cliniche, oltre alla persistenza a breve termine del virus
I limiti dello studio
1) Non sono stati testati campioni di siero per affrontare la viremia o le tendenze sierologiche. I motivi sono i risultati di tassi positivi al virus estremamente bassi nello studio iniziale (1 su 49 casi), che non forniscono alcuna conclusione stimata. Il test sierologico non è stato condotto perché non erano disponibili kit affidabili di IgM / IgG.
2) Non sono stati fatti l’isolamento del virus e i test di infettività dei campioni. Ci si è concentrati sulla stima della persistenza del virus SARS-CoV-2 in vari fluidi corporei tra i casi di COVID-19, ma ciò non implicava l’esistenza di particelle virali infettive.
3) Il numero di campioni mancanti era superiore a quanto programmato inizialmente nello studio, ciò è stato attribuito principalmente a basse percentuali di produzione di espettorato purulento nei casi di polmonite virale, nonché alla bassa compliance dei pazienti.
4) Questo studio può comportare errori di selezione poiché sono stati inclusi gruppi di casi di dimensioni modeste.
5) Assumendo che tutti i casi di COVID-19 presentassero SARS-CoV-2 in tutti i campioni all’inizio dei sintomi, la media e il 95^ percentile che avevano stimato erano più brevi del previsto a causa dell’incertezza del tempo di incubazione. Il tempo stimato in questo studio attraverso casi COVID-19 ospedalizzati potrebbe non essere generalizzabile a tutte le infezioni da SARS-CoV-2, come i casi asintomatici.
Raccomandazioni
In conclusione, i nostri risultati mostrano una persistenza prolungata di SARS-CoV-2 in pazienti ospedalizzati con COVID-19. Gli operatori sanitari dovrebbero considerare questi risultati nelle raccomandazioni diagnostiche e nelle misure di prevenzione circa il virus.
Fonti:
- Sun J, Xiao J, Sun R, Tang X, Liang C, Lin H, et al. Prolonged Persistence of SARS-CoV-2 RNA in Body Fluids. Emerg Infect Dis. 2020;26(8):1834-1838. https://doi.org/10.3201/eid2608.201097